
Bientôt un médicament créé par l’IA
Dans les bureaux d’Insilico Medicine, au centre-ville de Montréal, un scientifique nous fait une démonstration de l’une de leurs plateformes d’IA, capable d’imaginer en quelques étapes de nouvelles molécules pharmaceutiques.
Devant nous, il ajuste les propriétés d’une molécule comme on modifie les paramètres d’une image. Le programme génère de nouvelles molécules thérapeutiques, chacune optimisée selon des critères choisis : stabilité, efficacité, absorption.
L’entreprise Insilico Medicine, d’abord basée à Hong Kong, est la toute première à amener une molécule entièrement générée par IA jusqu’en phase II des essais cliniques, l’étape où l’on teste l’efficacité d’un traitement sur des patients humains.
Insilico Medicine fait partie de cette nouvelle vague de jeunes entreprises qui misent sur l’IA pour transformer la recherche pharmaceutique. Leurs promesses : radicalement réduire les délais, abaisser les coûts de développement de nouveaux traitements dans une des industries.
Je crois que nous sommes sur un point de bascule dans le domaine de la recherche pharmaceutique
, estime Petrina Kamya, biochimiste et présidente de la branche canadienne de la compagnie. Née en Ouganda, formée à Concordia, elle dirige le développement de leurs plateformes d’intelligence artificielle.
C’est aussi ce qu’espère Nicolas Moitessier. Professeur en chimie à l’Université McGill, il s’intéresse lui aussi au potentiel de l’IA pour la découverte de médicaments dans le cadre de sa recherche universitaire. Cela fait plus de 30 ans qu’il conçoit des molécules thérapeutiques et qu'il cherche des moyens d’accélérer leur découverte grâce aux outils informatiques.
On va pouvoir sauver des vies. Des patients qu’on aurait soignés dans dix ans pourront peut-être être traités l’année prochaine.

Nicolas Moitessier, professeur en chimie à l’Université McGill.
Photo : Radio-Canada
Le développement d'un nouveau médicament est une odyssée longue et coûteuse. Les estimations varient, mais on parle souvent de plusieurs milliards de dollars — entre 2 et 10 milliards — et de plusieurs décennies de travail. À commencer par la recherche fondamentale, pour comprendre les mécanismes d’une maladie.
Pour un médicament qui arrive sur le marché, on estime que les chercheurs évaluent environ 10 000 composés chimiques. Parmi ceux-là, une poignée – environ 250 – sont testés sur des animaux, avant que cinq seulement ne soient jugés assez prometteurs pour les essais cliniques sur l’humain.
À l’arrivée, un seul obtiendra l’approbation réglementaire. C’est ainsi qu’on développe des médicaments depuis des décennies.
Le potentiel de l’IA
À partir de 2012, des percées majeures bouleversent le domaine : des ordinateurs rivalisent avec les humains pour reconnaître des images, jouer au Go, comprendre des textes.
Là, tout d’un coup, l’intelligence artificielle est arrivée. Et on s’est dit : est-ce qu’on ne pourrait pas la faire penser autrement? Il y a eu un engouement très rapide, et les investissements ont suivi
, se rappelle Nicolas Moitessier. Ces entreprises nous disaient : donnez-nous votre problème, on va essayer de le régler.
C’est dans cette effervescence qu’est née Insilico Medicine, avec l’intuition que ces nouveaux outils pouvaient transformer radicalement la manière dont on conçoit des traitements, notamment contre les maladies liées au vieillissement.
Ce qui distingue leur approche d’autres jeunes pousses qui se sont lancées avec la même ambition, c’est l’objectif de couvrir l’ensemble du processus, de la découverte de la cible jusqu’aux essais cliniques.
Notre idée : créer des outils pour aider les scientifiques à surmonter tous les obstacles de la découverte de médicaments
, explique Petrina Kamya.

Petrina Kamya, biochimiste et présidente de la branche canadienne d'Insilico Medicine.
Photo : Radio-Canada
Au cours de la dernière décennie, la compagnie a développé trois grandes plateformes d’intelligence artificielle : l’une pour identifier les cibles biologiques, une autre pour générer de nouvelles molécules thérapeutiques, et une dernière pour prédire leurs effets cliniques potentiels.
Pour y parvenir, elle a produit des centaines de publications scientifiques validant ses approches. Le projet le plus avancé est celui d’une molécule destinée à traiter la fibrose pulmonaire idiopathique (FPI), une maladie dégénérative où le tissu pulmonaire se rigidifie graduellement sans cause connue.
La fibrose pulmonaire est une maladie mortelle. Sans traitement, les patients ont une espérance de vie d’environ trois ans
, explique le docteur Toby Maher, pneumologue de l’École de médecine Keck de l’Université de Californie du Sud.
Les deux médicaments actuellement disponibles ne font que ralentir la progression de la maladie. Ils ne permettent pas de la guérir.
Le docteur Maher parle en connaissance de cause. Il estime avoir dirigé plus d’une centaine d’essais cliniques de traitements visant à traiter la maladie.
Aucun n’a mené à un traitement. Ces essais cliniques coûtent très cher, et le docteur a surtout témoigné de leur coût humain. Les patients qui viennent me voir n’ont souvent aucune autre option de traitement, et quand un essai échoue, c’est une grande déception.
L’enjeu des bonnes cibles
Pourquoi tant d’échecs en essais cliniques? Dans bien des cas, c’est parce que le médicament n’agit pas sur la bonne cible.
C’est habituellement le travail des chercheurs universitaires : comprendre la maladie afin d’identifier quels mécanismes moléculaires font défaut, puis trouver sur quelles molécules, ou quelles cibles, agir pour développer un médicament : des protéines ou des gènes du corps humain sur lesquels un médicament pourrait agir.
C’est un processus long, complexe et incertain. L’intelligence artificielle peut l’accélérer, voire l’élargir.
Les modèles développés chez Insilico sont alimentés par une variété de données : publications scientifiques, séquences génétiques, résultats d’études cliniques, données issues de la génomique, de la transcriptomique et de la protéomique.
Il y a une multitude de données publiques qu’on peut exploiter pour identifier de nouvelles cibles thérapeutiques
, précise Kamya. Et les algorithmes d’apprentissage profond sont très efficaces pour intégrer ces sources disparates et faire émerger des corrélations que les humains ne peuvent pas percevoir.
L'identification de la cible thérapeutique est la première étape pour développer un médicament.
Photo : Radio-Canada
Pour la fibrose pulmonaire, la plateforme a comparé les profils génétiques de patients malades avec ceux de personnes en bonne santé. Elle a repéré plusieurs gènes surexprimés dans les tissus atteints. Pour chaque gène identifié, l’algorithme scanne ensuite la littérature scientifique pour voir lesquels ont déjà été associés à la maladie
, explique Petrina Kamya.
Plus le lien est documenté, plus la cible obtient un bon score. C’est une façon de rendre le processus plus objectif et plus quantifiable que ce que les chercheurs faisaient avant. Ensuite, vous sélectionnez les 5 ou 10 molécules qui ont obtenu la meilleure note, et vous les validez en laboratoire
, poursuit-elle.
Ces validations expérimentales ont lieu dans les installations de l’entreprise à Shanghai. C’est là qu’une cible en particulier a retenu l’attention : une protéine jamais visée auparavant pour cette maladie, mais dont le rôle dans les mécanismes du vieillissement était bien documenté.
Nous avions l’impression que nous aurions de meilleures chances de traiter cette maladie, ainsi que d’autres associées au vieillissement, en visant une cible à la fois impliquée dans la maladie mais aussi dans le processus de vieillissement
, explique Petrina Kamya.
Une approche jugée innovante par le Dr Toby Maher : À ma connaissance, personne d’autre n’a tenté de cibler cette voie pour traiter la fibrose pulmonaire.
Concevoir la bonne molécule
La cible thérapeutique est le point de départ pour la conception du médicament. Les chimistes parlent souvent d’une serrure dont il faudra forger la clé. Il leur faudra construire une molécule qui pourra s’attacher à la cible thérapeutique, afin d’en bloquer la fonction pour traiter la maladie.
Traditionnellement, les chimistes partent de bibliothèques contenant des millions, voire des milliards, de composés chimiques existants. Grâce à des techniques de modélisation, ils peuvent tester virtuellement leur compatibilité avec la cible visée.
Les meilleures candidates sont ensuite évaluées une par une par des chimistes qui, selon leur expertise, vont déterminer si elles valent la peine d’être achetées ou synthétisées.
Nous n’avons pas tous la même lecture d’une molécule
, explique Jérôme Genzling, doctorant dans le laboratoire de Nicolas Moitessier à l’Université McGill. Certains vont juger de sa facilité de synthèse, d’autres vont se concentrer sur ses interactions biologiques, ou encore sur ses propriétés physico-chimiques. Notre expérience influence ce qu’on considère comme prometteur.
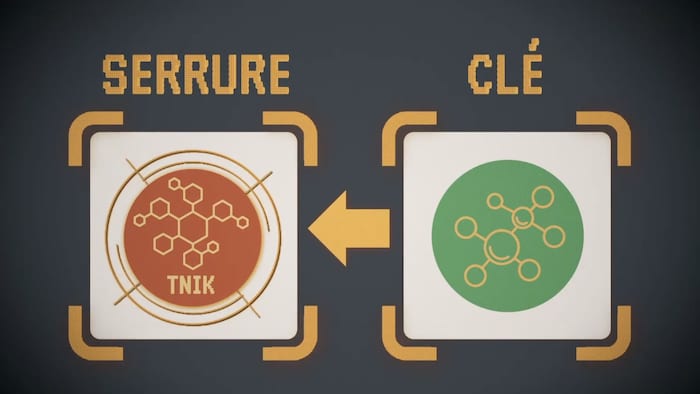
La cible, c'est celle-ci. C'est le point de départ des chimistes. Ils la comparent à une serrure, pour laquelle il faut forger une clé, construire une molécule médicamenteuse.
Photo : Radio-Canada
Jérôme Genzling reconnaît la subjectivité de leur évaluation. La première fois que tu regarderas la molécule, ça ne sera pas de la même manière que le lendemain.
Un bon médicament doit non seulement s’attacher à la protéine ciblée, mais la molécule doit aussi satisfaire une longue liste de critères : elle doit être non toxique, synthétisable, stable, bien absorbée et distribuée dans le corps, tout ça sans causer d’effets secondaires.
C’est pour ça que les molécules doivent être améliorées à l’ordinateur, puis testées en laboratoire, améliorées, puis testées… encore et encore. Un travail parfois presque artisanal. J'ai optimisé une propriété, mais j'en ai perdu une autre. J'ai réussi à optimiser une troisième propriété et j'ai perdu la première. Donc on fait ça de façon très itérative
, illustre Nicolas Moitessier.
Chez Insilico, au lieu de travailler avec des molécules existantes, les chercheurs misent sur l’intelligence artificielle générative. Cette même technologie qui crée des vidéos et des visages que vous n’avez jamais vus auparavant, nous l’utilisons pour créer des molécules que vous n’avez jamais vues non plus. Alors nous créons de nouvelles entités moléculaires
, résume Petrina Kamya.
Nous explorons les possibilités chimiques comme jamais auparavant. Nous ne sommes pas contraints par les limites subjectives et les biais que peuvent avoir les chimistes.
C’est dans ce contexte que Hugo de Almeida Silva, scientifique en conception de médicaments assistée par IA chez Insilico, nous fait une démonstration de la plateforme de génération de molécules.
La plateforme comprend 37 modèles prédictifs, qui peuvent prédire les caractéristiques chimiques et physiques des molécules générées, leur distribution dans le corps, leur solubilité, leur stabilité et les effets secondaires possibles. Dans le menu ici, on peut cliquer sur les propriétés que nous souhaitons améliorer, afin d’en faire un meilleur médicament. Ensuite, il va me générer des idées, des molécules différentes mais qui vont garder les propriétés qui sont importantes pour nous.

Hugo de Almeida, scientifique en conception de médicaments assistée par IA, à Insilico Medecine Canada.
Photo : Radio-Canada
Alors, commente Petrina Kamya, nous savons si ces molécules sont solubles, si elles seront bien distribuées dans le corps, si elles causeront certains effets secondaires spécifiques… avant même qu’elles soient synthétisées.
La biochimiste veut nous rassurer : Toutes les propriétés chimiques prédites par l’ordinateur doivent être vérifiées en labo, et si c’est confirmé, tant mieux. Sinon, on prend cette nouvelle information et on alimente le modèle informatique pour améliorer ses capacités prédictives.
Au terme de ce processus, Insilico a développé la molécule ISM001-055. Avant d’arriver en essais cliniques, nous avons synthétisé environ 75 molécules. Normalement, c’est des milliers de molécules. Ça nous a pris 18 mois. Normalement, ça prend 3 à 5 ans.
Les essais cliniques de phase II a sur 71 patients viennent d’être terminés. En 12 semaines, les patients ont vu une amélioration de leurs fonctions pulmonaires, ce que ne permet aucun médicament existant. Une réussite, du premier coup.
Le docteur Toby Maher, qui supervise les essais cliniques, est optimiste. Les données des essais cliniques d’Insilico sont incroyablement prometteuses. Ils pourraient avoir trouvé un premier traitement efficace contre la fibrose pulmonaire.

Le docteur Toby Maher, pneumologue de l’école de médecine Keck de l’Université de Californie du Sud.
Photo : Radio-Canada
Mais le médecin reste prudent, car les bénéfices doivent être confirmés lors des essais cliniques de phase III, avec plus de patients. Mais le simple fait qu'ils aient réussi à se rendre aussi loin, c’est mieux que ce que beaucoup d’autres ont tenté auparavant.
Des données limitées
Malgré l’enthousiasme, Nicolas Moitessier reste prudent. On a sans doute exagéré les capacités de l’IA au tout départ. Beaucoup de start-ups sont arrivées avec des promesses trop ambitieuses, parfois sans même l’expertise en pharmaceutique. Mais aujourd’hui, la hype est passée, et on est plus réalistes.
Par ailleurs, le chercheur observe un frein potentiel au développement de l’industrie : le manque de données expérimentales chimiques de qualité pour entraîner les modèles. Les entreprises sont en train de se rendre compte qu’il faudra mener beaucoup de tests coûteux pour obtenir davantage de données sur les propriétés des molécules.
Voilà pourquoi il explore de nouvelles approches à l’Université McGill pour contourner le problème, en combinant l’IA à des approches plus classiques et en développant des modèles qui intègrent les lois de la chimie, en plus des données massives.
En gros, on enseigne la chimie à l’ordinateur comme on le ferait avec un étudiant : on ne lui donne pas juste des réponses, on lui explique les principes, dit-il. Le processus est plus lent, mais potentiellement plus robuste.

Des chercheurs à l'oeuvre dans les laboratoires de Nicolas Moitessier.
Photo : Radio-Canada
Des traitements plus accessibles?
En ce moment, Insilico Medicine a 31 autres molécules en cours de développement, dont huit sont en essais cliniques. Certains en oncologie; d’autres sont des anti-infectieux contre la COVID.
C’est un portfolio diversifié parce que nous voulons faire la démonstration des possibilités de cette approche
, explique Petrina Kamya. Si une petite biotech comme nous pouvons avoir un pipeline si garni, développé en seulement quatre ans, imaginez ce que de plus grosses compagnies peuvent faire.
Pour la biochimiste, il est impératif que la technologie se démocratise, afin de pouvoir aussi traiter des maladies plus rares ou qui sévissent dans des pays qui ont moins l'attention des chercheurs et des compagnies pharmaceutiques
À Montréal, le professeur Nicolas Moitessier explore lui aussi les possibilités de l’intelligence artificielle au sein de sa propre entreprise, Molecular Forecaster.
Je pense que l’intelligence artificielle va complètement transformer notre façon de faire de la recherche en médecine. On va découvrir des médicaments plus rapidement, pour un plus grand éventail de maladies, et à un coût bien moindre. Et si on réussit à faire baisser le coût du développement, c’est le patient qui en bénéficiera. J’aime rêver à ça.
Advertising by Adpathway























